Електролітична дисоціація: Пояснення феномену розпаду молекул на іони
Електролітична дисоціація — це ключовий процес, який спостерігається у розчинах електролітів та визначає їхні властивості провідності. Це явище полягає в розпаді молекулярних сполук на заряджені частинки — іони, під дією електричного струму чи зміни умов середовища.
Основи Електролітичної Дисоціації
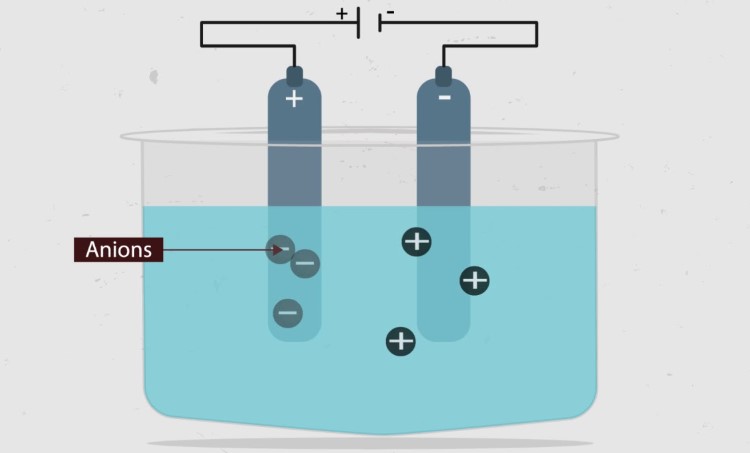
У розчинах електролітів молекули розчиненої речовини розділяються на іони, які можуть бути позитивно зарядженими (катіони) або негативно зарядженими (аніони). Цей розпад відбувається під впливом електричного поля або взаємодії з розчинником.
Механізм Дисоціації
Розпад молекул на іони може відбуватися у залежності від типу електроліту:
- Сильні електроліти: Це сполуки, які повністю розпадаються на іони у розчині під впливом електричного струму. Прикладами є солі та кислоти.
- Слабкі електроліти: Ці речовини лише частково дисоціюються, їхня реакція на електричне поле є менш інтенсивною. Наприклад, деякі органічні кислоти або деякі солі.
Вплив Факторів на Дисоціацію
Різні фактори можуть впливати на електролітичну дисоціацію:
- Температура: Зазвичай підвищення температури збільшує ступінь дисоціації електроліту.
- Концентрація розчину: Збільшення концентрації може змінити ступінь дисоціації.
- Тиск: У випадку газоподібних електролітів, тиск може впливати на їхню розчинність та дисоціацію.
Використання в Науці та Повсякденному Житті
Електролітична дисоціація відіграє важливу роль у різноманітних наукових дослідженнях, особливо в хімії та фізиці розчинів. Це явище також має практичне застосування у технології, зокрема, у виробництві електролітичних розчинів, батарей, а також у водопідготовці та інших сферах.
Електролітична дисоціація є важливим процесом, який дозволяє розуміти поведінку електролітів у розчинах. Це явище має значення як для наукових досліджень, так і для технологічних застосувань, створюючи фундаментальну базу для розуміння характеристик різних речовин у розчинному стані.
теги: Що таке електролітична дисоціація